2018美国药典多肽药物质量与标准国际论坛
USP International Forum on Therapeutic Peptides Quality and Standards 2018
多肽指由氨基酸经过肽键连接在一起而形成的化合物,通常意义上超过四十个氨基酸的称为蛋白,而小于四十个氨基酸的称为多肽。多肽药物的发展由来已久,其范围可以囊括合成多肽,重组多肽甚至是胰岛素类产品。进入二十一世纪以后,随着生物技术以及生物医药的迅猛发展,多肽药物也得到快速发展,全球的多肽药物市场预计将会超过250亿美元。中国作为原料药生产大国,越来越多的企业开始进入多肽药物领域。但是,由于其分子量介于传统小分子化药与生物大分子药物之间,加之生产工艺的多样性,导致多肽药物的质量研究以及标准制定存在诸多困难,如何做好多肽药物的质量研究,进而确定相应的质量标准已成为业界最关心的话题之一。
美国药典委员会 (USP) 作为全球领先的药物质量标准制定机构,本次特别邀请海内外标准设定机构、法规监管、多肽研发、生产等专家共聚一堂,将与您共同交流和讨论多肽药物中国前景与机遇、GMP生产与法规、多肽药物质量研究的技术发展、多肽药物的药典标准更新以及杂质的分析技术和质控标准。
学习目的
主题会议:
• 美国药典委员会在中国的十年:质量与合作
• 美国药典的生物标准开发进展
• 美国药典委员会生物1(多肽和胰岛素)专家委员会的活动与更新
一.多肽药物在中国的前景与机遇
• 中国多肽药物及胰岛素的市场分析与展望
• 中国多肽药物的发展与机遇
二.多肽药物及其相关杂质的分析表征与质控技术
• 合成及重组多肽药物的分析表征技术及生物评价方法
• 多肽药物定量研究中灵敏度与选择性的综合考量
• 合成多肽药物的质量控制策
• 多肽质量研究对工艺优化的指导
• 多肽及生物制品质量控制中高场核磁的应用及案例分析
三.多肽药物的药典标准及更新
• 美国药典多肽药物各论概述
• USP合成多肽的质量控制策略 - 白皮书及更新
• 多肽药物的临床前药学研究
• 胰岛素产品的质量控制策略
• 中国药典多肽及胰岛素标准更新(拟定)
• 满足各国药典要求的胰岛素及类似物的表征研究
四.多肽药物生产与质量的法规考量
• 美国多肽仿制药的科学及法规考量
• 多肽药物的国内外同步注册策略
• 多肽药物杂质研究的挑战及美国药典多肽药物杂质标准开发更新
• 多肽药物生产的GMP规范
• 美国FDA的GMP现场核查
• GMP生产中合成多肽药物原物料的质量控制策略
(会议主题可能更新,请以现场发布为准)
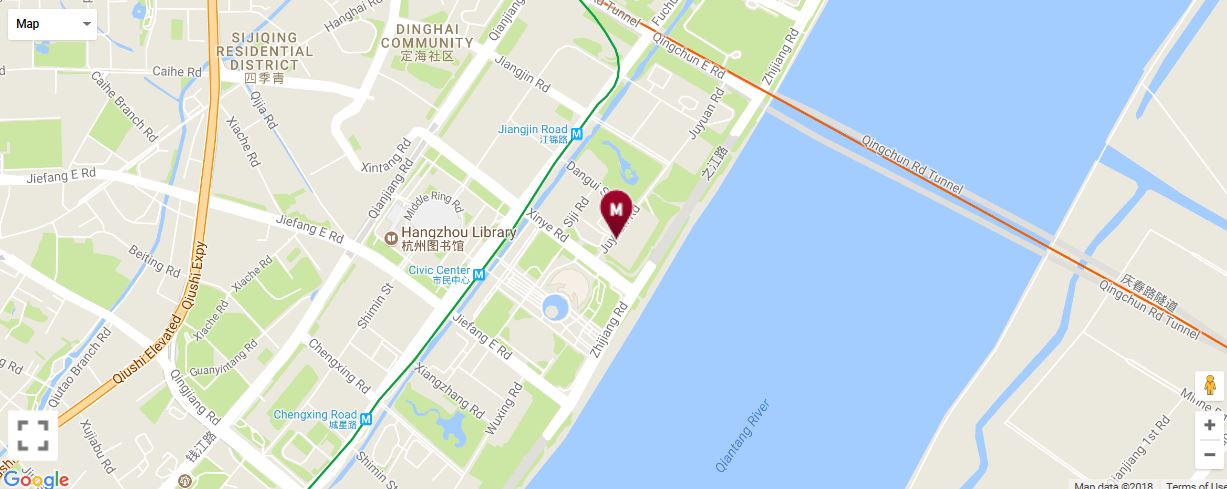
交通路线:地铁4号线(彭埠方向)江锦路站(A1口出),步行700米
-
操洪欣先生美国药典委员会中华区,战略客户发展部高级总监
-
Michael De Felipps博士美国药典委员会生物1(多肽和胰岛素)专家委员会主席
-
Kevin Carrick博士美国药典委员会,全球生物部门总监
-
Manoj Kumar Metta博士美国药典委员会,全球生物部门科学与标准事务联络人
-
Jeff Jiang博士美国食品药品监督管理局 (US FDA),药物评价与研究中心,研究与标准/仿制药办公室,治疗性能部门,副主任
-
陶剑虹女士国家食品药品监督管理总局南方医药经济研究所副所长、《医药经济报》总编
-
徐寒梅博士中国药科大学教授,国家药典委员会委员,中国药科大学多肽药物创制工程研究中心主任
-
陶安进博士深圳翰宇药业股份有限公司,研发副总裁
-
唐洋明先生深圳翰宇药业股份有限公司,研发部经理
-
姜建军博士海南双成药业股份有限公司,多肽原料药副总裁
-
潘俊锋先生成都郑源生化科技有限公司,总经理
-
Michael S. Verlander美国药典委员会生物1(多肽和胰岛素)专家委员会副主席
-
Loren Olson先生上海爱博才思分析仪器贸易有限公司 应用与市场开发高级研究员
-
许金峰先生中肽生化有限公司 研发副总
-
单璐博士布鲁克(北京)科技有限公司 应用经理
-
阮宏强先生上海中科新生命生物科技有限公司 副总经理
-
陆军波先生中肽生化有限公司 质量副总
-
谈技女士上海昂博生物技术有限公司 总经理
-
更多演讲专家正在更新中......

• 在线报名网址:www.echinachem.com/events/2018usp/register.html
• 报名联系人:王艳红 / Nina Wang,手机:13884941886(微信同号),Email:yanhong.wang@echinachem.com
| 国内参会机构Domestic Participant Type | 参会费用Standard Registration Rates | 会前付款Advance Registration Rates | 早鸟优惠(截止:2018.2.9)Early Bird Discount until Feb. 9 |
|---|---|---|---|
| 企业 Industries | 4000元/人 | 3700元/人 | 3400元/人 |
| 政府机构 Government | 3200元/人 | 3000元/人 | 2800元/人 |
| 科研院校 Research Institutes | 2200元/人 | 2000元/人 | 1800元/人 |
| 海外参会机构Overseas Participant Type | Standard Registration Rates | Advance Registration Rates | Early Bird Discount until Feb. 9, 2018 |
| Industries | 600 USD | 550 USD | 500 USD |
| Government | 500 USD | 450 USD | 400 USD |
| Research Institutes | 350 USD | 300 USD | 250 USD |